تشخیص نوروپاتی فیبر کوچک
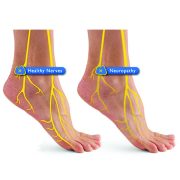
فیبرهای عصبی نازک میلیندار (A-delta) و فیبرهای عصبی بدون میلین (C)، مسئول ادراک دما، درد و عملکرد خودکار هستند. نوروپاتی فیبر کوچک (SFN) که مربوط به اختلال عملکرد و یا از دست دادن این فیبرها است، از جمله ناهنجاریهای بالینی رایج محسوب میشوند که منجر به کاهش قابل توجهی در کیفیت زندگی میشوند. اختلالات حسی به علت آسیب فیبرهای کوچک و یا از دست دادن آنها، شامل علائم منفی (thermal cutaneous hypoesthesia) و علائم مثبت مانند (درد سوزش خوبهخودی یا هایپرآلرژی یا thermal allodynia) میشوند. انواع مختلفی از شرایط پاتولوژیک ممکن است باعث ایجاد SFN شود، از جمله علل متابولیک (دیابت و یا اختلال تعادل گلوکز)، علل عفونی (کمبود ایمنی بدن یا عفونت ویروس هپاتیت c)، علل سمی (شیمی درمانی یا الکل)، و علل ژنتیکی (آمیلوئیدوز یا بیماری فابی). از آنجا که مطالعات هدایت عصبی رایج (NCS) و بیوپسی عصب تنها فیبرهای بزرگ عصبی را بررسی میکنند، SFN مدتها به عنوان یک مسئله حل نشده و چالش باقی مانده است. تاکنون بسیاری از آزمایشات برای تشخیص SFN صورت گرفته است. در این مطالعه معیار تشخیصی چهار مورد از این آزمایشات در بیماران SFN یا احتمال بیماری در آنها، مقایسه شده است. آزمونهای مورد مطالعه شامل: آزمون کمّی حس (QST) برای حسهای حرارتی. از جمله آستانه تشخیص گرما و سرما (WDT,CDT)، ثبت پتانسیل تحریک شده با لیزر (LEP)، اندازهگیری هدایت الکتروشیمیایی پوست (ESC) و ثبت پاسخ سیناپتیک پوست (SSR). این مطالعه در بیمارستان هنری مونور فرانسه نیز تایید شده است. در این مطالعه 87 فرد با احتمال بروز به SFN و یا بیمار دارای SFN دردناک که از نظر بالینی مشخص شده است مورد بررسی قرار گرفتند. این افراد در معاینات بالینی علائم عینی تغییرات فیبر بزرگ نداشتند و پارامترهای NCS ایشان در حالت نرمال بوده است.
آزمون کمّی حسی (QST)
QST بر روی پشت دست (عصب شعاعی) و پاها (عصب پرایمر سطحی) در هر دو طرف انجام میشود. آستانههای تشخیص گرما و سرما توسط محرکهای Peltier متصل به آنالایزر سنسور حرارتی انجام میشود. پس از یک دوره تنظیم با دمای خنثی 32 درجه سانتیگراد، درما تا 0 درجه کاهش و یا تا 50 درجه افزایش مییابد تا زمانی که بیمار دکمه پاسخ سیگنال را فشار دهد.
پتانسیل برانگیخته لیزری (LEP)
LEP با استفاده از یک لیزر CO2 که دست و پار را تحریک میکند، ثبت میشود. هر محرک شامل یک پالس حرارتی شعاعی خفیف است (طول موج: 10.6 mm، توان 9w و قطر پرتو: 3.5 mm). طول پالس برای هر بیمار بین 10 تا 30ms تغییر میکند تا بتواند حس دردناک را ایجاد کند.
پاسخ سیناپتیک پوست (SSR)
پاسخ سیناپتیک پوستی در کف دستها و پاها پس از تحریک الکتریکی عصب trigeminal، ثبت میشود. الکترودهای مرجع در پشت دست و پا قرار میگیرند. سه آزمایش با استفاده از افزایش شدت و فواصل تحریک به طور تصادفی برای جلوگیری از عادت، انجام میشود. دامنه (حداکثر پیک) و تاخیر بهینه برای ثبت بهترین پاسخ در نظر گرفته میشود.
هدایت الکتروشیمیایی پوست (ESC)
این آزمایش با استفاده از سودواسکن صورت میپذیرد که عملکرد اعصاب سودوموتور مورد ارزیابی قرا میگیرد. کف دست و پاهای بیمار بر روی صفحه الکترود فلزی قرار میگیرد. سپس ولتاژ کمتر از 4 ولت به ان اعمل میشود. با توجه به تعریق کف دستها و پاها هدایت الکتروشیمیایی تغییر کرده و ثبت میشود.
با توجه به نتایج این تحقیق، در میان روشهای موجود LEP و ESC از حساسیت بالاتری برای تشخیص تخریب فیبرهای کوچک برخوردار بودند. همچنین بر اساس این مطالعه، ارزیابی ESC در مقایسه با سایر آزمونهای اعصاب خودکار قابلیت اعتماد بیشتری برای عملکرد سودوموتور در تشخیص زودهنگام نوروپاتی محیطی به همراه دارد. که حتی برخی از افراد مورد مطالعه کوچکترین علائم بالینی برای نوروپاتی محیطی نداشتند. علاوه بر این، بر خلاف آزمون رفلکس آکسون سودوموتور کمّی ((Quantitative sudomotor axon reflex test)QSART)، که آزمون زمانبری برای تست اعصاب خودکار است، این روش کمتر از سه دقیقه انجام میشود و قابلیت تکرار دارد.




دیدگاه خود را ثبت کنید
Want to join the discussion?Feel free to contribute!